CASOS CLINICOS 2010
PREMIO PNEUMA-SOCALPAR (600,-€)
-1-
MASA MEDIASTÍNICA
Dr. D. José Antonio Pinto Blázquez
SOCIEDAD DE PREVENCIÓN DE IBERMUTUAMUR DE CÁCERES.
Varón de 35 años. Comercial de productos agrícolas. Acude a consulta por disnea de esfuerzo.
Antecedentes familiares: sin interés. Antecedentes personales:
– Exfumador de 10 paquetes / año desde hace 4 años.
– Hernia de hiato.
– Amigdalectomizado, apendicectomizado e intervenido de desviación de tabique nasal y pólipos nasales.
– Tratamiento médico: omeprazol 20 mg. ocasionalmente.
Enfermedad actual: hace un mes, comienza con fiebre, tos, disnea y aumento de expectoración, por lo que recibe antibioterapia de amplio espectro durante 10 días a nivel ambulatorio, persistiendo en la actualidad disnea de esfuerzo. Clínica habitual de reflujo gastroesofágico.
Exploración física: Peso: 96 Kg., talla: 1.76 cm., TA 120 / 70. Normal.
Analítica: Hemograma: normal; Coagulación: normal; Bioquímica: ácido úrico: 7.4, albúmina 5.2 y GGT 62. Resto normal.
Espirometría: FVC 3640 (75%), FEV1 3030 (75%), FEV1/FVC 83. Test broncodilatador negativo.
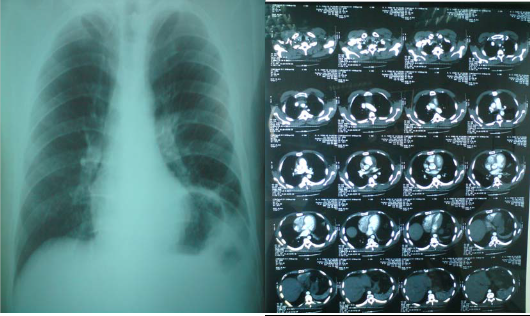
Saturación de oxígeno: 97 %. Gasometría arterial: pH: 7.40, PaO2 96, PaCO2 43. Radiografía de tórax (2P): elevación del hemidiafragma izquierdo.
TAC torácico: Masa mediastínica anterior, con pequeñas áreas quísticas, sin signos de invasión local.
Radioscopia: parálisis hemidiafragmática izquierda. Hemidiafragma derecho con movimiento conservado.

Juicio clínico: Masa mediastínica anterior.
Tratamiento: se comenta en sesión médico-quirúrgica, y se decide intervención quirúrgica, la cual se realiza sin complicaciones postoperatorias.
Diagnóstico anatomo-patológico: Timoma.
-2-
NEUMONÍAS DE REPETICIÓN EN LII EN PACIENTE ¿POR QUÉ?
Autor: Dra. Mª Isabel Ramos Cancelo
Hospital Santa Bárbara de SORIA
Paciente de 21 años sin alergias medicamentosas conocidas. Sordera neurosensorial en seguimiento por ORL. Neumonías de repetición desde la infancia, siempre localizadas en LII. Diagnosticado de asma leve intermitente en seguimiento por Neumología. En tratamiento inhalado solamente en agudizaciones. Estudiante de Medicina
Remitido a Consultas Externas de Neumología tras un episodio de neumonía adquirida en la comunidad, estando resuelta en el momento de acudir a Consulta .En el momento de acudir a Consulta presentaba una exploración física normal y refería que los cuadros cursan con fiebre elevada sin tos ni expectoración. Presenta en Rx de tórax áreas sugestivas de bronquiectasias por aumento de trama broncovascular en LII por lo que se solicita TACAR torácico : Alteración de la morfología cardiaca con aparente aumento
de cavidad ventricular izquierda. En el parénquima pulmonar no se identifican bronquiectasias y únicamente llama la atención de la existencia de áreas de enfisema centrolobulillar únicamente situadas en LII. Además aparentemente saliendo de la aorta torácica parece identificarse una estructura vascular que irriga dicha base pulmonar
.Estos hallazgos de vaso anómalo junto con los cambios enfisematosos son compatibles con secuestro pulmonar extralobar. La espirometría se encontraba dentro de la normalidad
Tras ser realizado TAC, presenta en Octubre de 2009 otro episodio neumónico en LII
con buena respuesta a tratamiento ambulatorio con Levofloxacino (aporta RX .Fig 1 y
1a).Con los hallazgos previos se solicitó:
– Angioresonancia magnética torácica para valoración de estructuras vasculares anómalas en el contexto de secuestro pulmonar
– Ecocardiograma por aumento de tamaño de cavidades izquierdas (descartar efecto shunt acompañante)
Se realiza Angioresonancia magnética torácica y angio de aorta torácica, donde se aprecia una zona de consolidación parenquimatosa en LII adyacente a la aorta descendente. No se aprecian alteraciones en mediastino ni adenopatías. En el estudio de AngioRNM de aorta torácica se aprecia un vaso anómalo que sale de la aorta descendente e irriga a la zona de consolidación parenquimatosa del lóbulo inferior izquierdo. No se aprecian otras alteraciones en aorta ni en sus ramas a nivel torácico. Conclusión: lesión en LII con vaso anómalo compatible con secuestro pulmonar (Fig 2
y Fig. 3)
El Ecocardiograma transtorácico mostraba unas cavidades de tamaño y morfología normal, en todo caso AD algo dilatado; el ventrículo derecho es normal. No se objetivan flujos anormales. Sin anomalías valvulares; únicamente insuficiencia tricuspídea fisiológica que permite cálculo de PAPs : 30-35 mmHg
Se trata por lo tanto de un paciente joven con neumonías de repetición siempre localizada en LII (dos en este año, con buena respuesta a tratamiento ambulatorio antibiótico); con funciones pulmonares normales; secundarias a un secuestro pulmonar con irrigación anómala dependiente de aorta torácica. Se remite a Consultas Externas de Cirugía Torácica para valoración de resección de la lesión, estando en el momento

actual pendiente de intervención quirúrgica.
Fig 1 y 1ª. Rx de uno de sus procesos neumónicos
Fig 2 : RNM : Consolidación parenquimatosa en
LII adyacente a Aorta torácica con vaso anómalo
Fig 3 : AngioRNM de aorta torácica se aprecia un vaso anómalo que sale de la aorta descendente e irriga a la zona de consolidación parenquimatosa del lóbulo inferior izquierdo

DISCUSIÓN :
El secuestro pulmonar es una Malformación congénita caracterizada por tejido embrionario quístico no funcionante con vascularización de una arteria sistémica anómala; con la peculiaridad de que el tejido pulmonar no se comunica con el árbol bronquial. Se trata de patología rara (representa el 0,5-6% de todas las malformaciones pulmonares) que afecta al 0,15-1,7% de la población general. Con frecuencia se localizan en el pulmón izquierdo y en los lóbulos inferiores (60-90%),pero pueden verse en cualquier lóbulo, incluir todo el pulmón o situarse debajo del diafragma simulando
un tumor abdominal. Su vascularización depende en su mayor parte de la aorta torácica (74%) seguido de la aorta abdominal (21%) y de otros vasos (5% de arterias mamarias internas, subclavia, intercostales, faringea inferior, gastrica izquierda, arterias renales y coronarias) ; y su drenaje venoso a través de arterias pulmonares, ácigos, hemiácigos o sistema porta (por lo que pude producirse cortocircuito izquierda –derecha)
La mayoría de ellos se diagnostican en la infancia, por que generalmente y sobre todo los extralobares se asocian a otras malformaciones congénitas como por ejemplo, fístulas traqueoesofágicas o gástricas, anomalías diafragmáticas, quistes pericárdicos, duplicación de colon o de ileon terminal ó anomalías de vértebras cervicales. Clínicamente cursan con neumonías de repetición siempre en la misma localización que se caracterizan por escasa expectoración, debido a que no tienen comunicación con el árbol bronquial; con clínica de absceso pulmonar y en casos más graves con hemoptisis o insuficiencia cardiaca si existe una fístula arteriovenosa.
Pueden clasificarse en :
1. Típicos o completos: si presentan tejido pulmonar e irrigación aberrante a) Extralobares : aislados de las estructuras pleuropulmonares normales formando territorios aberrantes, estando totalmente revestidos de pleura
b) Intralobares : incluídos en el parénquima pulmonar normal sin revestimiento pleural
2. Atípicos o incompletos : si sólo presentan uno de los dos componentes El diagnóstico se basa en la clínica acompañado de técnicas de imagen donde el AngioTAC o la AngioRNM son de gran utilidad para valoración de estructuras vasculares anómalas; siendo la Aortografía torácica el “gold standard”. El tratamiento es siempre quirúrgico con ligadura del vaso nutricio y lobectomía (toracotomía o videotoracoscopia)
BIBLIOGRAFÍA:
1. Reina Álvarez .Secuestro pulmonar intralobar.Presentación de un caso y revisión de literatura.Revista Electrónica de Portales Médicos. Com
2. González R, Saldías R, Alarcón E et cols. Secuestro pulmonar: 8 casos Rev Chilena de Cirugía VOL 56 N ª3 Junio 2004 :pag 237-242
3.Sabbaghi E. Caso Radiológico Adultos. Rev Chil Enf Resp 2005 ; 21 :42-43
-3-
CASO CLÍNICO SOCALPAR 2010
Autores: C. Ainhoa Arroyo Domingo, Julio De Frutos Arribas, Félix Del Campo Matías, Ana Mª Andrés Blanco, J.Luis Carretero Sastre, Tomás Ruiz Albi. Servicio de Neumología. Hospital Río Hortega. Valladolid.
Hombre de 73 con hemoptisis.
Paciente de 73 años, exfumador de 40 paq/año, hipertenso, sin tratamiento habitual ni patología respiratoria previa. Acude al hospital por un cuadro de tos con expectoración amarillenta y ocasionalmente hemoptoica de 10 días de evolución. No refería disnea, dolor torácico ni costal. No sudoración nocturna, anorexia ni astenia. Había iniciado tratamiento antibiótico en su domicilio, sin presentar mejoría.
En la exploración física, presentaba buen estado general, constantes normales. Destacaba en la auscultación la presencia de crepitantes en campo superior izquierdo y algún roncus aislado, encontrándose el resto de la exploración dentro de la normalidad.
Exploraciones complementarias:
-Rx tórax: patrón alveolo-intersticial en LSI y LID. (Foto1).
-Analítica: VSG 28, PCR 14, S.Sangre 10.000 Leucos (60%N), Hb 9,1, Hto 17,6%,Hm
3.210.000, PQ 327.000. Bioquímica: glucosa, función renal, hepática, iones y ferritina normal. Estudio de inmunidad: ANA, ANCA y Ac. Anti Mb negativos. Proteinograma e inmunoglobulinas, normales. Marcadores tumorales normales. Serología de bacterias atípicas normales.
-Ecocardiograma: cavidades cardiacas de tamaño normal. VI con función sistólica global y segmentaría normal. Válvulas normales. Ausencia de derrame pericardio. No datos indirectos de HTP.
-Fibrobroncoscopia (el primer día de ingreso) sangrado global en todo el árbol bronquial de predominio izquierdo, sin poderse establecer de donde proviene el sangrado. Morfología del árbol bronquial normal. No imágenes de tumoración ni infiltración de la mucosa. Repetida, a la semana del ingreso: árbol bronquial con secreciones hemorrágicas recientes y antiguas algunas coaguladas. Morfología del árbol bronquial normal. Se hace BAL de língula superior con 3 x 50 ml, recuperándose bien
70 ml hemáticos algo oscuros. Se recoge BAS: leucocitos, PMN y células escamosas con abundantes macrófagos, algunos de ellos con hemosiderina, junto con células cilíndricas ciliadas de vías respiratoria bajas en atípica. Negativo para células tumorales. BAL: El estudio en la cámara de Neubawer, revela 28.160 células x mc, de las cuales el
99% son hematíes. El resto de las cámaras, muestra un fondo hemático e inflamatorio de predominio agudo, con numerosos macrófagos espumosos, muchos de ellos cargados de hemosiderina y de forma aislada, alguna célula escamosa de aspecto habitual. Biopsia bronquial y transbronquial: fragmentos de mucosa bronquial y parénquima pulmonar sin evidencia de infiltración neoplásica.
-TAC Toráco-abdominal: infiltrado alveolo-intersticial distribuido de manera difusa y asimétrica en ambos campos pulmonares con mayor afectación del LSI, estructuras mediastinicas sin alteraciones (Foto 2). Masa adrenal izquierda de 8 x9 cm que presenta densidad heterogéneo con calcificaciones, componente quístico y septos, hiposólidos que muestran realce significativo. Muestra extensa superficie de contacto con la arteria renal izquierda, sin poderse descartar infiltración. La masa muestra también una
superficie de contacto sin plano graso de separación con la cola del páncreas, sin poder descartar infiltración.
-Exp.Funcional: Espirometría: FVC=2.28 (70%).FEV1=1.69 (79%). FEV1/VC=74%. MMEF 25-75=46%.Difusión:DLCO=6.62 (89%).DLCO/VA=1.48 (121)%.
Evolución
Durante el ingreso el paciente recibe tratamiento antibiótico y antitusígeno, con buena respuesta clínica, cediendo completamente la hemoptisis y la tos. Tras la realización de la FBS se inicia tratamiento con corticoides ante la sospecha clínica de hemorragia alveolar difusa (HAD). Se da el alta al paciente, para seguimiento ambulatorio hasta la intervención, siendo valorado a los 5 días en la consulta externa, requiriendo nuevo ingreso ante el empeoramiento radiológico y analítico del paciente. Este precisa la trasfusión de 4 concentrados de hematíes por Hb 6.9.Hto 21.9. Se realiza arteriografía bronquial: aortografía de aorta torácica, se identifica las arterias bronquiales de tamaño y morfología normales. Se intenta hacer estudio superselectivo de arterias bronquiales de pulmón izquierdo con varios catéteres específicos para las mismas y solo se consigue embolizar las arterias bronquial inferiores del pulmón izquierdo. Tras la realización de esta técnica el paciente permanece asintomático desde el punto de vista del sangrado bronquial, mejorando clínicamente. Posteriormente es intervenido por Urología donde se le realiza una suprarrenectomia laparoscópica. Tras esta el paciente comienza con hemoptisis masiva, que precisa intubación y conexión a ventilación mecánica, intentándose realizar cauterización del sangrado con fibrobroncoscopia y sonda de Fogarti, no siendo posible. Presentando los días siguientes hemorragia pulmonar masiva y distress respiratorio con posterior shock hipovolémico y exitus.
Tras el fallecimiento del paciente se realizó la autopsia, siendo el diagnostico:
angiosarcoma de glándula suprarrenal izquierda con infiltración de la grasa periadrenal y metástasis pulmonares con hemorragia pulmonar masiva.
Discusión
El angiosarcoma es una neoplasia maligna del endotelio vascular o linfático que representa el 2% de todos los sarcomas de tejidos blandos. El angiosarcoma comúnmente afecta a piel, tejidos blandos, corazón, mama o riñón. Independientemente del lugar de origen, las metástasis pulmonares son particularmente probables, aunque es muy difícil el diagnóstico anatomo-patológico. La HAD es una presentación infrecuente del angiosarcoma, existiendo solo unos pocos casos en la literatura. La HAD es un síndrome clínico que tiene diversas etiologías inmunes y no inmunes. Dentro de las
causas inmunes las vasculitis, LES, síndrome de Goodpasture y hemosiderosis
pulmonar idiopática, son los más frecuentes. Las principales causas no inmunes son principalmente las inducidas por fármacos, o las debidas a tumores malignos hematológicos y los trastornos de la coagulación. Se caracterizan por la presencia de hemoptisis, anemia ferropénica e insuficiencia respiratoria aguda. El diagnóstico habitualmente se realiza en base a los hallazgos clínicos, de laboratorio y radiológicos, resultando la Fibrobroncoscopia de gran utilidad. El lavado broncoalveolar puede mostrar eritrocitos en el episodio agudo de la hemorragia y macrófagos cargados con hemosiderina en el sangrado crónico. El síndrome de hemorragia alveolar difusa es una patología grave, que pone en serio riesgo de vida al paciente, llegando incluso en muchos casos a la asistencia respiratoria mecánica y posterior fallecimiento del paciente, por lo que su diagnóstico debe ser planteado rápidamente para poder iniciar el tratamiento y mejorar el pronóstico.
La hemorragia alveolar difusa es una forma de presentación infrecuente del angiosarcoma, tanto del pulmonar primario, como del metastático, debiéndose incluir en el diagnóstico diferencial de DAH.


Foto1. Radiografía de tórax PA: patrón alveolo-intersticial en LSI y LID.
Foto 2.TAC torácico: infiltrado alveolo-intersticial distribuido de manera difusa y asimétrica en ambos campos pulmonares.
-4-
Caso clínico SOCALPAR: HEMOPTISIS CATAMENIAL.
Autores:García R, Bernabé MJ ,Cordovilla R , Márquez JV , Torrachi AM. Servicio de Neumología. Hospital Clínico de Salamanca
Mujer de 24 años de edad , estudiante universitaria, que presenta episodios de hemoptisis recidivante en los dos últimos años. La cuantía de la misma es de 10-15 cc al día. De vez en cuando se acompaña de sensación de opresión torácica.
Acude por primera vez a su médico de atención primaria en abril del 2006 por un cuadro de tos con expectoración hemoptoica y fiebre. La exploración física, la radiografía de tórax y la revisión de ORL fueron normales , ante la sospecha de un cuadro infeccioso respiratorio recibió antibioterapia de forma empírica.
Tras varios episodios de características similares es derivada a Neumología para realizar un estudio completo de la hemoptisis.
En cuanto a la historia clínica no tenía antecedentes de enfermedades cardiopulmonares ni de tromboembolismo, tampoco alergias conocidas. Negaba el consumo de tabaco, alcohol o drogas . Su examen físico resultó de nuevo normal, al igual que la función pulmonar y la radiografía de tórax. Los cultivos microbiológicos de esputo ,incluido el BK, resultaron negativos y en la tomografía axial computarizada ( TC ) de tórax no se evidenció patología. Las pruebas de laboratorio de rutina, las pruebas de anticuerpos antinucleares, factor reumatoide, anticuerpo citoplasmático antineutrófilo y anticuerpos antifosfolípidos estaban dentro de límites normales. La broncoscopia flexible no mostró ningún punto de sangrado.
Durante su seguimiento en consulta persistieron los episodios de hemoptisis; en una de las revisiones la paciente refiere haberse dado cuenta de que la hemoptisis aparece en el primer día del ciclo menstrual y que tras dos o tres días cede de forma espontánea. Ante la sospecha de endometriosis pulmonar se le realiza una nueva broncoscopia y una TC durante la menstruacción, además es derivada a ginecología para valoración. No presentaba clínica sugerente de endometriosis pélvica ; la exploración y la eco ginecológica resultaron normales.

La TC realizada durante el ciclo menstrual puso de manifiesto una infiltración mal definida del lóbulo inferior derecho (Figura 1). La exploración broncoscópica flexible llevada a cabo durante el mismo período, no mostró ningún punto de sangrado, pero reveló una marcada hiperemia difusa que afectaba a carina y al bronquio principal izquierdo (Figura 2). En el lavado bronquial y en el cepillado no se encontraron células endometriales.

La paciente comenzó tratamiento con anticonceptivos orales con una resolución total de sus síntomas . Tras seis meses no ha vuelto a presentar hemoptisis.
![]()
FIGURA 1: vídrio deslustrado en LID
FIGURA 2 : hipervascularización en carina
DISCURSIÓN:
La endometriosis se define como la presencia de tejido endometrial funcional en regiones extrauterinas. Aunque la endometriosis suele limitarse a la pelvis, también puede afectar a órganos extrapelvicos como el pulmón. La endometriosis pulmonar es una patología rara que se caracteriza por la presencia de tejido endometrial funcional dentro de la pleura, el parénquima pulmonar o las vías respiratorias. El tejido es sensible a las hormonas sexuales circulantes por lo que las manifestaciones clínicas están relacionadas con el ciclo menstrual. La la hemoptisis catamenial es un síntoma raro, con pocos casos descritos en la literatura. La sospecha clínica y establecer la relación temporal de los síntomas con la menstruación es esencial para realizar el diagnostico.
Los hallazgos de la tomografía axial computarizada (TC) pueden ser: opacidades, lesiones nodulares, cavidades de paredes finas y formaciones ampollosas. Debe realizarse durante la menstruación para que la sensibilidad diagnóstica sea máxima. La utilidad de la broncoscopia es limitada, porque en la mayoría de los casos de endometriosis torácica está implicado el parénquima distal siendo el examen broncoscópico normal. En raras ocasiones, al comienzo de la menstruación, se objetivan focos de endometriosis en las vías aéreas centrales en forma de manchas
aisladas violáceas o rojizas y lesiones quísticas en la submucosa. Desaparecen después de la menstruación aunque puede quedar una cripta como signo de curación de los quistes.
La confirmación histopatológica es difícil, sólo se ha conseguido en un tercio de los casos.
Existe controversia en cuanto al tratamiento adecuado , se ha empleado terapia hormonal, resección pulmonar o simplemente el seguimiento de los pacientes.
La inhibición farmacológica de las hormonas sexuales con la hormona liberadora de gonadotropina (GnRH) es el tratamiento de elección para la endometriosis pulmonar ya que tiene la misma eficacia que en la endometriosis pélvica. El problema es que los síntomas reaparecen tras su suspensión y dado que estos fármacos inhiben la ovulación, los pacientes que desean concebir a veces se niegan a someterse a esta terapia . Otros fármacos suprimen el tejido endometrial como el danazol o la progesterona provocando un estado de pseudoembarazo.
Las indicaciones de la cirugía pulmonar son: fracaso de la terapia hormonal, efectos secundarios intolerables o recurrencia de los síntomas tras la interrupción del tratamiento médico. Cuando las lesiones son múltiples o no se localizan, la ooforectomía puede ser una opción. Por otro lado, la cirugía debe ser el método de elección si la paciente desea quedarse embarazada. Para las lesiones periféricas la resección en cuña mediante toracoscopia video-asistida es el método preferido. En los pacientes con endometriosis bronquial central puede ser necesaria la subsegmentectomía, la segmentectomía o incluso la lobectomía.
CONCLUSIONES:
Los síntomas relacionados con la endometriosis torácica son muy diversos y por lo general se refieren al sitio donde se localiza el endometrio ectópico. La endometriosis torácica se puede sospechar en mujeres en edad reproductiva con hemoptisis, incluso en ausencia de síntomas de endometriosis pélvica.
El diagnóstico de la endometriosis torácica generalmente se basa en los síntomas clínicos, ya que los procedimientos de localización incluyendo la endoscopia en muchos casos no son diagnósticos.
![]()
El tratamiento médico consiste en análogos de la GnRH. El tratamiento quirúrgico se emplea en los casos de fracaso del tratamiento médico o la reaparición después de la interrupción del tratamiento. La ooforectomía bilateral puede ser considerada si la afectación pulmonar es multifocal o irresecable.
-5-
Titulo: TOS CRÓNICA EN PACIENTE CON COLITIS ULCEROSA
Autores: Vicente Roig Figueroa, Águeda Herrero Pérez
Servicio de Neumología. Hospital Clínico Universitario. Valladolid
Caso clínico: Mujer de 37 años de edad, con antecedentes de Colitis ulcerosa (1999), síntomas extraintestinales en 2000 (eritema nodoso, artralgias y uveitis) y Pancolectomia (2006).
La paciente fue estudiada en otro hospital por tos seca de un año de evolución. La tos fue inicialmente esporádica, haciéndose progresivamente continua e invalidante, tanto nocturna como diurna. No se acompañaba de disnea, sibilancias, opresión torácica, hemoptisis ni síntomas generales. A la exploración, paciente eupneica, sin cianosis ni acropaquias digitales. Auscultación cardiopulmonar normal, no edemas en miembros inferiores. Saturación transcutánea de Oxígeno: 97%

Exámenes complementarios practicado en su centro de referencia: analítica hemática estandar: dentro de la normalidad. Electrocardiograma: ritmo sinusal a 80 por minuto. Rx de Tórax: sin alteraciones de interés. Espirometría: parámetros espirométricos dentro de la normalidad. Examen microbiológico de esputo no crecimiento bacteriano ni de hongos. Baciloscopia no BAAR. Cultivo de micobacterias negativo. Prueba broncodilatadora negativa. Se inició tratamiento con formoterol y budesonida, no obteniendo ninguna mejoría, por lo que
se solicita TAC torácico convencional y de alta resolución que es normal y test de provocación bronquial con metacolina que resulta negativo. La paciente es remitida desde su hospital de origen a nuestra consulta de Neumología. Se efectúa broncoscopia, apreciándose una mucosa traqueal difusamente engrosada y eritematosa, con pérdida del relieve de los cartílagos traqueales. Se aprecian además múltiples imágenes nodulares,
milimétricas, también en toda la longitud de la tráquea. Abundantes secreciones traqueales y fibrina (fotografía 1) Carina traqueal y ambos árboles bronquiales sin alteraciones. El estudio microbiológico del broncoaspirado para bacterias, hongos y micobacterias resultó negativo. La biopsia traqueal mostró engrosamiento de epitelio de superficie con intensa inflamación crónica y pequeñas áreas de microabscesificación. No se observan granulomas necrotizantes, ni signos de malignidad. Las células no expresan Virus de papiloma humano. No se observa crecimiento bacteriano, micobacteriano ni de hongos. Técnica de Rojo congo: negativa. Se evidencian algunos rasgos histopatológicos sugestivos de papilomatosis. Se realizó nueva broncoscopia con cepillado traqueal para estudio del virus del papiloma humano mediante PCR, que resultó negativa. La serología para VIH, VHB y VHC resultaron también negativas. Autoanticuerpos antitejido, ANA y ANCA negativos. Estudio funcional respiratorio con espirometría, prueba broncodilatadora, volúmenes pulmonares estáticos y transferencia de CO dentro de la normalidad. En el test de marcha de 6 minutos la paciente recorrió
740 metros sin desaturación durante el esfuerzo. Se practicó nuevo TAC cervico- torácico apreciandose una discreta irregularidad en pared posterior de tercio distal de tráquea.
Diagnóstico: Traqueitis fibrinonodular difusa asociada a Colitis ulcerosa.
Evolución: Se pauta tratamiento con prednisona a dosis de 1mg/kg/día y fluticasona a dosis de 1000 microgramos día. La paciente experimenta una mejoría espectacular con
desaparición de la tos a las 2 semanas de instauración del tratamiento, permaneciendo asintomática desde entonces, con dosis decrecientes de corticoides orales. Se repitió broncoscopia a los tres meses de inicio del tratamiento, desapareciendo por completo las

lesiones descritas previamente (foto 2) Discusión: La afectación traqueal aislada es excepcional en la enfermedad inflamatoria intestinal. La imagen endoscópica suele ser el de una mucosa inflamada, a veces hemorrágica, nodular y fibrinosa. El diagnóstico diferencial endoscópico se plantea con la tuberculosis y la aspergilosis traqueal, la policondritis recidivante, la amiloidosis traqueobronquial, y la vasculitis de Wegener. Más raramente puede remedar una papilomatosis traqueal. Los
corticoides inhalados habitualmente no son suficientes para el control de la enfermedad, precisando corticoides orales para su manejo. La respuesta clínica y endoscópica habitualmente es satisfactoria, si bien hay casos descritos de estenosis traqueal severa que precisaron dilataciones endotraqueales.
Bibliografía:
1.Black H et al. Thoracic Manifestations of Inflammatory Bowel Disease. Chest
2007;131;524-532
2.T. Kuzaniar et al. Severe tracheobronchial stenosis in a patient with Crohn’s disease. Eur
Respir J 2000; 15: 209-212
PREMIO PNEUMA-SOCALPAR(600,-€) MEDICO RESIDENTE.
-1-
HEMOPTISIS EN MUJER DE 52 AÑOS.
Autor: Aníbal Manuel Hernández Gil .Residente de tercer año de Neumología del
Hospital Marqués de Valdecilla. Santander
Anamnesis
Mujer de 52 años que es enviada por su médico de cabecera por tos y hemoptisis. Alérgica a paroxetina No tenia hábitos tóxicos ni factores de riesgo cardiovascular conocidos. Presentó cólicos nefríticos de repetición en su adolescencia .Estudiada en Cardiología por disnea y dolor torácico con pruebas complementarias normales. Seguida en Consulta de Medicina Interna por aftas orales recurrentes, lumbalgia y poliartralgias con estudios negativos para conectivopatías. En seguimiento por Digestivo por epigastralgia , naúseas y pirosis con todas las pruebas de nuevo negativas. Síndrome del ovario poliquístico seguida en Consultas de Ginecología. Síndrome depresivo.
Intervenciones quirúrgicas: amigdalectomía en la infancia y hemmorroidectomia. Tratamiento habitual: antidepresivos, ibuprofeno y omeprazol.
Enfermedad actual.
La paciente acude remitida por su médico de cabecera por cuadro de 1 mes de evolución de esputos hemoptoicos casi diarios coincidentes con accesos de tos y con 4-5
episodios de hemoptisis franca de escasa cuantía (20-25 ml). No presentaba sensación distérmica ni fiebre termometrada , no dolor torácico . No astenia, anorexia ni pérdida de peso. No clínica gastrointestinal ni genitourinaria. No alteraciones cutáneas ni neurológicas. Su médico de Atención Primaria le solicito una radiografía de tórax que fué informada como normal. Dada la persistencia de la hemoptisis es derivado a la Consulta de Neumología.
Exploración física.
Paciente consciente y orientada en persona, tiempo y espacio. Buen estado general. Normohidratada y normoperfundida. Eupneica en reposo.
Cabeza y cuello: sin alteraciones de interés. Tórax normoconformado.
Auscultación cardiaca: rítmica sin soplos ni extratonos. Auscultación pulmonar: ruidos respiratorios normales.
Abdomen y extremidades inferiores: sin alteraciones.
Pruebas complementarias.
Hemograma: normal. Bioquímica : normal. Actividad de protrombina: 96%.Ziehl y BK
de esputo: negativo.
Fibrobroncoscopia: se objetivan restos hemáticos por todo el árbol bronquial , con datos de sangrado activo a nivel del LSI. Excrecencia de la mucosa de consistencia dura a nivel de porción distal de bronquio principal izquierdo que se biopsia a la espera de anatomía patológica definitiva.
Radiografía de tórax: realizada el mismo día de la broncoscopia que es normal. TAC torácico: citado para una semana después de realización de broncoscopia.
Evolución y comentarios.


Tras la realización de la broncoscopia la paciente refiere aumento de la tos y de la expectoración hemoptoica , malestar general y sensación distérmica sin fiebre termometrada por lo que a la espera del TAC se le realiza radiografía de tórax( figura 1) Posteriormente se le realiza TAC torácico( figura 2) en el que se visualiza un llamativo engrosamiento de la pared traqueal , del bronquio principal izquierdo y de las ramas
Figura1.Se observa infiltrado a nivel de segmento anterior Figura 2. Engrosamiento de la pared bronquial del principal y
del lóbulo superior izquierdo no presente en radiografía de ramas lobares del árbol bronquial izquierdo con calcificación
previa y clara estenosis de la luz..
lobares de ese lado con calcificación y estenosis de la luz sugestivos de afectación localizada de traqueobroncopatía osteocondroplástica junto a un infiltrado alveolar en segmento anterior del LSI. La paciente es tratada con antibióticos con mejoría de la
clinica y del infiltrado radiológico en pocos días . Posteriormente nos llega el resultado de la anatomía patológica de la lesion biopsiada en el bronquio principal izquierdo confirmando el diagnóstico de traqueobroncopatía osteocondroplástica . La paciente actualmente esta asintomática y hace vida normal.
Discusión.
La traqueobroncopatía osteocondroplástica es una rara enfermedad benigna (frecuencia del 0,11%) de etiología desconocida que afecta al sistema endobronquial , fundamentalmente a tráquea y bronquios proximales respetando típicamente la parte membranosa. Se da con más frecuencia en varones. Se caracteriza por el depósito de fosfato cálcico en la submucosa de las vías aéreas de mayor calibre, que condiciona una proliferación de tejido óseo y cartilaginoso dando lugar a la formación de nódulos endobronquiales que protruyen en la luz bronquial. Se han descrito posibles asociaciones con sarcoidosis, policondritis, traqueobroncomalacia, asma, rinitis o carcinoma epidermoide pulmonar pero no han podido ser corroboradas dada la poca prevalencia de la enfermedad. En un porcentaje importante de los casos se descubre al
realizar una broncoscopia por otros motivos o por la aparición de disnea (por afectación traqueal importante), tos crónica, infecciones pulmonares o hemoptisis. En nuestro caso han aparecido paulatinamente casi todas las formas de presentación, primero
hemoptisis y tos recurrente y posteriormente neumonitis distal como consecuencia del proceso obstructivo.
En cuanto al tratamiento no hay un consenso al respecto. Casi todos los autores están de acuerdo en no tratarla si los síntomas del paciente no le condicionan una mala calidad
de vida o infecciones recurrentes. Para estos casos se opta por la escisión de los nódulos con broncoscopia rígida, colocación de stents bronquiales, ablación por láser, reseccion quirúrgica (incluso neumonectomía para afectaciones muy extensas) o tratamiento con radioterapia cuando ninguna de las intervenciones anteriormente descritas pueden realizarse o el paciente no puede ser operado.
Bibliografía.
Tracheobronchopathia Osteochondroplastica: Presentation of ten cases and review of the Literature. Jabbardarjani et als. LUNG 2008 186:293297.
BioqueC., Feu N et al Tracheobronchopathia Osteochondroplastica: clinical study and follow-up in nine cases.J. Bronchol 8:78-83.
Sofía Alsina Sarmiento y cols. Traqueobroncopatía osteocondroplástica. Rev Cubana
Oncol 2(16):88-92.
Dutau H., Musani A (2004)Treatmente of severe Tracheobronchopathia
Osteochondroplastica, J. Bronchol 11:182-185.
-2-
TÍTULO: CASO CLINICO ACERCA DE UN CASO DE DERRAME PLEURAL.
Autores: C.A. Amado, J. Villuela, Residentes Neumología HUMV Santander
Paciente mujer de 45 años que ingresa desde urgencias para estudio por derrame pleural
Antecedentes Personales
NAMC, Fumadora de 20 Paquetes-año. HTA en tratamiento. Melanoma cutáneo resecado en 2001.
Enfermedad Actual
Clínica consistente en 3 semanas de evolución de febrícula que dos semanas después se acompañó de dolor torácico izquierdo tipo pleurítico y moderado deterioro del estado general. Tras acudir por 2ª vez a urgencias es ingresada con la presencia de derrame
pleural izquierdo. Con tos y expectoración mucopurulenta escasa. Disnea de moderados
esfuerzos. No edemas o tumefacción en MMII, no oliguria. No otra focalidad infecciosa. Niega presencia de artritis.
Exploración Física
TA 120/70 FC10 lpm Tª36,5 ºC frecuencia respiratoria de 26 rpm, consciente, orientada, obesa, CC no estasis yugular, Tórax: forma no alterada, simétrica, dinámica sin alteraciones, tono mate a la percusión en campos pulmonares medios y basales de hemitorax izquierdo. A. Cardiaca: tonos rítmicos, sin soplos, taquicardia. A. Pulmonar: hipoventilación en campos medios e inferiores de hemitorax izquierdo, con disminución de transmisión de vibraciones vocales. Abdomen: blando, sin masas. EEII: no edemas
no signos de flebitis, pedios positivos no datos de trombosis venosa profunda.
Datos Complementarios
21300 leucocitos 78% p y C 11% pasando al alta a 5600 leucocitos P 67% Hb 11,3
Dímero D 5000 VSG 129 TP 73% Cr. 0,8; PCR 15 pasando en el ingreso a 2,3; CA
125:42 ANA y FR negativos. ANCA negativos microalbuminuria 52, mantoux negativo T4l, TSH, CEA, CA15,30, CA19.9 AFP, proteinograma, lactato, enz cardiacas, normales.
Gasometría arterial PO2 66 pCO2 35, pH 7,41 SatO2 95%
RX Tórax: no cardiomegalia, velamiento difuso en base y campo medio pulmón izquierdo, no estando completamente libre en decúbito lateral izquierdo. Ausencia de alteraciones a nivel de parénquima derecho. Sin significativa desviación parenquimatosa a pesar de cuantía del derrame. Al alta aclaración significativo del derrame pleural, persistiendo láminas de derrame en base y campo medio izquierdos.
Líquido pleural: pH 7, glucosa 19, LDH 2500, ADA 31, colesterol 89, triglicéridos 40, gram: no se observan gérmenes, cultivo aerobio y legionella negativo, BAAR negativo, PCR M. tuberculosis negativo. 320 células por mililitro con 30% macrófagos, 30% linfocitos y 30% polimorfonucleares. 10% células mesoteliales.
Hemocultivos negativos
Cultivo de esputo: negativo
Antígeno de legionella y neumococo negativos
Serología fiebre Q, legionella negativos
IgG Positiva con IgM negativa para Micoplasma pneumoniae
EKG RS a 86 lpm, eje normal, sin alteraciones significativas.
(Realizado antes de toracocentesis)AngioTAC torácico: derrame loculado en hemitorax izquierdo con atelectasia subyacnte sin signos de TEP Pequeña atelectasia basal derecha por parálisis frénica derecha.
Juicio Diagnóstico
Derrame pleural izquierdo complicado complejo de origen infeccioso
Evolución, Tratamiento y Conclusiones
Se trata de un caso clínico acerca de una mujer fumadora y obesa y sedentaria con clínica consistente en febrícula de 3 semanas de evolución que presenta derrame pleural izquierdo, de tipo exudado, loculado, en cuya situación clínica destaca lo larvado del proceso infeccioso y la buena tolerancia clínica de la paciente, a pesar de tratarse un derrame de cuantía moderada y loculado. Se descartó la etiología tuberculosa mediante cultivo de esputo, mantoux, prueba de la tuberculina y ADA de líquido pleural. Se descartó la presencia de un Tromboembolismo pulmonar, debido a los resultados obtenidos en la gasometría, y a la aparición relativamente brusca de dolor torácico, motivo por el que se realizó angio-TAC, que no evidenció datos de tromboembolismo pulmonar, pero sin embargo permitió objetivarse claramente que se trataba de un derrame loculado (que ya se podía prever en la radiología simple). A pesar de los resultados negativos a la hora de filiar la etiología exacta del proceso, debido a los
resultados analíticos (leucocitosis con predominio leucocitario) y del análisis del líquido pleural (con pH de 7 y análisis AP), se asume la etiología infecciosa del proceso. Para el tratamiento se inició terapia antimicrobiana de amplio espectro y se colocó tubo de tórax, mediante guia ecográfica, realizándose tratamiento mediante fibrinolisis con uroquinasa durante 3 días con las dosis habituales. Tras este tratamiento se objetivó buena evolución del derrame, estando en estado residual al alta de planta y con buena evolución clínica 15 días después del alta. Se trata en definitiva de un derrame pleural izquierdo complicado complejo (según la clasificación de las guias de la SEPAR), de etiología probablemente bacteriana de presentación larvada.
Se adjuntan placas de derrame. La primera de ellas (figura 1) al ingreso de la paciente y la segunda (figura 2) al alta, tras retirada de tubo de tórax y fibrinolisis.
Figura 1:

-3-
TOXICIDAD PULMONAR Y CARDIACA POR TRATAMIENTO ANTIPARKINSONIANO
Autores: Muñiz González Francisco, García García Silvia
Anamnesis: Mujer de 74 años que acude por disnea. No refiere alergias medicamentosas conocidas. No hábitos tóxicos. Trabajó como costurera. Hernia inguinal izquierda intervenida hace 5 años. Enfermedad de Parkinson diagnosticada hace 6 años en seguimiento por Neurología. En tratamiento con SINEMET® (Carbidopa/Levodopa), SOGILEN® (Cabergolina) y MIRAPEXIN® (Pramipexol).
Enfermedad actual: La paciente refiere un aumento progresivo de disnea hasta hacerse de esfuerzo durante aproximadamente 3 años hasta que 15 días antes del ingreso se vuelve de reposo. Además asocia en los últimos días molestias faríngeas inespecíficas, disminución de la diuresis y edemas en miembros inferiores. No fiebre, ni dolor torácico ni otra sintomatología asociada.
Exploración física: TA 120/60. Afebril. Hábito asténico. Normocoloreada de piel y mucosas. No se palpaban adenopatías periféricas. Exploración neurológica normal. Taquipneica en reposo. Presión venosa yugular elevada. Auscultación rítmica sin soplos. Auscultación pulmonar con crepitantes finos bibasales. Abdomen sin hallazgos. Extremidades inferiores con edemas con fóvea hasta las rodillas y pulsos periféricos presentes.
Pruebas complementarias:
Hemograma: hemoglobina 12.3, hematocrito 43 %, 8100 leucocitos (fórmula normal), plaquetas 359000. Estudio de coagulación normal.
Bioquímica: Urea, Creatinina, iones y perfil hepático dentro de la normalidad. EKG: ritmo sinusal sin alteraciones de la repolarización.
Radiografía de tórax: Cardiomegalia. Patrón alveolo-intersticial de predominio en lóbulos superiores y mínimo pinzamiento de ambos senos costo-frénicos.
TC toraco abdominal: Derrame pleural bilateral con afectación de pleura mediastínica. Extensas lesiones que predominan en lóbulos superiores con áreas de vidrio deslustrado y engrosamiento intersticial compatible con fibrosis sin poder descartar insuficiencia cardiaca. Cardiomegalia con crecimiento de aurícula derecha.
Ecocardiograma: Insuficiencia aórtica ligera-moderada. Ligera dilatación de cavidades derechas.
Evolución:
Aunque las pruebas de imagen resultaban un tanto confusas, atendiendo a la clínica de inicio de la paciente se instaura tratamiento diurético. Dada la buena evolución durante el ingreso con este tratamiento, se diagnostica de insuficiencia cardiaca congestiva y se da de alta.
Al mes acude de nuevo a Urgencias con una clínica similar consistente en disnea progresiva, ortopnea y edemas en miembros inferiores. En la Radiografía de tórax se
evidencia una cardiomegalia y zonas de patrón reticular en ambas bases pulmonares. Se
realiza una TAC torácico de alta resolución (figura 1) en la que se ven zonas parcheadas de patrón reticular en la zona periférica subpleural de ambos campos pulmonares, con mayor afectación de pulmón derecho. Acompañadas de bronquiectasias de tracción y distorsión de la arquitectura parenquimatosa. Además discreto patrón en mosaico con zonas de opacidad en vidrio deslustrado. Todo ello compatible con fibrosis pulmonar con zonas de posible actividad.
Se realiza un nuevo ecocardiograma transtorácico y transesofágico (figura 2) en el que a diferencia del anterior se observa una válvula aórtica trivalva, con un diámetro en senos de valsalva de 28 mm (dilatado para la superficie corporal de la paciente). Además se detecta un flujo de regurgitación central, significativo, con gran ocupación del tracto de salida que todo ello se traduce en una insuficiencia aórtica severa.
Figura 1. TACAR toraco abdominal Figura 2. Ecocardiogramatransesofágico

Ante este nuevo ingreso, teniendo en cuenta la afectación cardiaca y pulmonar, la primera posibilidad diagnostica es la de amiloidosis con afectación cardiaca y
pulmonar. Para su confirmación se realiza PAAF de grasa subcutánea siendo ésta positiva para depósito de amiloide. Sin embargo se comenta el caso con Hematología, que tras la realización de Gammagrafía con Tecnecio 99, Biopsia rectal y estudio de médula ósea, todas ellas negativas, se descarta esta posibilidad.
Tras la revisión de la literatura, existen casos descritos de la relación entre el tratamiento antiparkinsoniano, concretamente con Cabergolina y la aparición de valvulopatías y fibrosis pulmonar. Se comenta entonces el caso con Neurología y se decide la sustitución de la medicación en cuestión.
Desde entonces ha transcurrido un año de seguimiento en consulta mejorando significativamente el estado de la paciente, con resolución del patrón intersticial en la radiografía de tórax y reducción de la severidad de la valvulopatía aórtica. Desde ese momento el estado de la paciente se mantiene estable sin presentar agudizaciones ni ingresos durante un año.
Diagnóstico: Toxicidad por Cabergolina consistente en valvulopatía aórtica severa y fibrosis pulmonar, con episodios de insuficiencia cardiaca asociada.
Discusión: Varios artículos en la literatura demuestran una relación entre el tratamiento con agonistas dopaminérgicos derivados de la ergolina en el desarrollo, tanto de fibrosis pulmonar como extrapulmonar. En nuestro caso, la concomitancia de fibrosis pulmonar y de valvulopatía aórtica con el fármaco en cuestión, ambos descritos en varios casos clínicos publicados, y la mejoría, tanto en pruebas de imagen como clínicamente tras su retirada, hacen que se plantee un diagnóstico razonable de relación.
Bibliografía:
1. Cardiac and noncardiac fibrotic reactions caused by ergot-and nonergot- derived dopamine agonist. Andersohn F, Gorbe E. Mov Disord 2009; 24(1):129-33.
2. Toxicidad pleuropulmonar precoz asociada al tratamiento con Cabergolina, un fármaco antiparkinsoniano. Villavicencio C, Ramirez-Sarmiento A. Arch Bronconeumol. 2007 Sep; 43(9): 519-22.
3. Retrospective evaluation of cardio-pulmonary fibrotic side effects in symptomatic patients from a group of 234 Parkinson´s disease patients treated with cabergoline. Dhawan V, Medcalf P, Stegie F. J Neural Transm. 2005 May;
112(5): 661-8.
-4-
DOLOR ABDOMINAL EN TRASPLANTADA PULMONAR
Autores: Carmen Casillas, Aníbal Hernández, Beatriz Abascal, Alejandro Daly. Servicio de Neumología del Hospital Marqués de Valdecilla. Santander.
Paciente mujer de 56 años. Dudosa alergia a B-lactámicos. Ex fumadora de 5 paquetes/año desde hace 8 años. Enfermedad por reflujo gastroesofágico (ERGE). Obstrucción crónica flujo aéreo severo e insuficiencia respiratoria hipoxémica en relación con bronquiolitis obliterante por lo que se realiza trasplante bipulmonar. Como complicaciones más importantes presenta: neumotórax a tensión en hemitórax derecho, parálisis diafragmática derecha, rechazo agudo A3BO y miopatía esteroidea, con buena evolución posterior y alta.
A las 4-5 semanas del trasplante acude al primer control en consulta estando asintomático desde el punto de vista respiratorio con leve dolor en relación con toracotomía y en fosa renal derecha. Exploración física: hipofonesis en base de hemitórax derecho. Resto de exploración y control analítico normales.
Pasadas 2 semanas acudió al Servicio de Urgencias por un cuadro brusco de dolor abdominal en epigastrio irradiado en cinturón con náuseas y vómitos. En la exploración física presenta abdomen blando, depresible, doloroso en epigastrio a la palpación, con ruidos hidroaéreos diminuidos y sin signos de peritonismo. Radiografía de abdomen y analítica (incluida amilasa) sin alteraciones por lo que se decide alta.
Tras este cuadro disminuye progresivamente la intensidad del dolor, aunque persiste en hipocondrio derecho, acompañándose de náuseas, anorexia y ritmo intestinal normal, siendo las pruebas de función hepática normales en todo momento. En exploración abdominal destaca dolor en hipocondrio derecho con ausencia de ruidos hidroaéreos pero sin signos de peritonismo y Murphy negativo. En este momento se decidió la realización de una ecografía y un TAC abdominal, siendo estos los hallazgos:

Juicio diagnóstico: Neumatosis de colon ascendente con neumoperitoneo sin signos peritoníticos.
Evaluada por el Servicio de Cirugía General se decidió ingreso para vigilancia y cirugía. En intervención (realizada 2 meses después del trasplante) se objetivó neumatosis masiva del colon derecho y ángulo hepático, incluyendo el meso, y se realizó hemicolectomía derecha con anastomosis ileocólica laterolateral.
Resultado de anatomía patológica: Neumatosis quística intestinal (ileon terminal, apéndice cecal y colon derecho). Lipomatosis submucosa de colon y apéndice cecal. Hiperplasia lipomatosa de válvula de Bauin.
En el postoperatorio presentó como complicaciones hematoma de pared abdominal con pequeña dehiscencia, empeoramiento de ERGE y leucopenia e insuficiencia renal aguda en relación con inmunosupresión y profilaxis antiviral, ambas resueltas en el momento del alta.
Actualmente, desde el punto vista gastrointestinal, únicamente presenta clínica en relación con ERGE con una buena evolución del injerto pulmonar.
-5-
VARON DE 66 AÑOS CON DISNEA PROGRESIVA Y SINTOMAS RESPIRATORIOS INESPECIFICOS DE VARIAS SEMANAS DE EVOLUCION.
Autores: Sara Miranda Riaño, Dagoberto Bejarano Ugalde, Enrique Macías Fernández, David Vielba Dueñas, Santiago Juarros Martínez, Jorge Arana Ruiz.
Hospital Clínico de Valladolid, Servicio de Neumología
Anamnesis:
Varón de 66 años, sin alergias medicamentosas conocidas, exfumador desde hace 16 años (consumo acumulado 30 paquetes/año). Antecedente de EPOC severo e HTA en tratamiento habitual con Fluticasona/Salmeterol 25/250 mcg y Candesartán/Hidroclorotiazida 16/12,5 mg.
Acude al Servicio de Urgencias tras presentar varias semanas de aumento de disnea habitual, tos con escasa expectoración blanquecina y sin fiebre, que no presenta mejoría tras tratamiento ambulatorio con antibióticos y corticoides inhalados.
Exploración física:
Paciente, consciente, orientado, colaborador, tensión arterial 176/109 mmHg, frecuencia cardiaca 110 latidos al minuto, temperatura 36,7ºC, pulsioximetría basal 64% que mejora hasta el 95% con oxígeno de alto flujo con Ventimask® al 50% a 15 litros por minuto y tratamiento broncodilatador. Cuello simétrico, sin masas palpables. No se palpan adenopatías en región cervical, axilar o inguinal. Ruidos cardiacos arrítmicos sin soplos. Pulmones con roncus y sibilancias bilaterales, con disminución de murmullo
vesicular en mitad inferior de hemitórax derecho. Abdomen blando, depresible, no
doloroso a la palpación superficial ni profunda, sin visceromegalias palpables. Extremidades inferiores sin edemas, signo de Homans negativo.
Pruebas complementarias:
-Analítica y bioquímica sanguínea: hemoglobina 16,9 g/dL, hematocrito 54,8%, leucocitos 10820 mm³ (neutrófilos 78,10%), plaquetas 149,000 mm³, urea 67 mg/dL, creatinina 1,1 mg/dL, glucemia 135 mg/dL, sodio 144, mEq/L potasio 5,4 mEq/L. Gasometría arterial: pH: 7,31, pCO2 74,5 mmHg, pO2 40 mmHg, sO2 68,4%, HCO3c
36,4 mmol/L. Coagulación y Dímero D: normales. Marcadores tumorales: negativos.
-Pruebas funcionales respiratorias: capacidad vital forzada (FVC) 1710 ml (45,8%), volumen espiratorio forzado en el primer segundo (FEVı) 770 ml (26,5%) con prueba broncodilatadora positiva (FEVı) 970 ml (33,3%), Índice de Tiffenau 44,97%, Pico flujo espiratorio (PEF) 2360 ml (30,4%), volumen residual (RV) 2850 ml (116,2%), capacidad pulmonar total (TLC) 4820 ml (74,1%), cociente RV/TLC 148,8%, factor de transferencia del monóxido de carbono (DLCO) 25,38%, cociente DLCO/volumen alveolar 108%. Prueba de la marcha de los seis minutos (6MWT): distancia recorrida
360 m, pulsioximetría al inicio de la prueba 93%, pulsioximetría al final de la prueba
94%.
-Electrocardiograma: ritmo de fibrilación auricular con frecuencia cardiaca 110 latidos al minuto, sin trastornos de la repolarización.
-Radiografía posteroanterior y lateral de tórax: presencia de una gran opacidad homogénea en mitad inferior del hemitórax derecho con pérdida de volumen. No hay desplazamiento traqueal ipsilateral o contralateral ni parece existir derrame pleural. Se revisan radiografías torácicas previas de dos años antes, sin observarse alteraciones.

B Figura1. Radiografía antero- posterior (A) y lateral (B) al momento del ingreso. Se aprecia un gran aumento de densidad homogéneo y pérdida de volumen en hemitórax inferior derecho.
-TAC toracoabdominal: evidencia una gran masa de 20 x 23 x 26 cm (largo- anteroposterior-ransversal) en mediastino anterior que alcanza hasta el mediastino posterior, con densidad grasa y contenido heterogéneo, con tabiques en su interior de densidad de partes blandas y alguna calcificación puntiforme. No presenta un claro plano de separación con las estructuras mediastínicas (corazón, grandes vasos y bronquios), presentando inversión diafragmática y colapsando el lóbulo inferior derecho y parcialmente del lóbulo medio. Abdomen sin hallazgos relevantes.
-Fibrobroncoscopia: compresión extrínseca de lóbulo medio y lóbulo inferior derecho, sin lesiones endoluminales, tomándose una muestra de broncoaspirado para estudio de Citología, que es informada negativa por células malignas.
-Resonancia magnética de tórax: se descarta infiltración a arteria pulmonar y vena cava superior, aunque sin descartarse infiltración a pericardio por ausencia de un claro plano de separación entre este y la tumoración.
-Gammagrafía ósea: sin evidencia de metástasis óseas.
-Punción – aspiración con aguja fina (PAAF) transtorácica guiada por escáner torácico: se obtienen muestras de material no valorable para el diagnóstico, por lo que se decide nuevamente repetir la fibrobroncoscopia e intentar punción transbronquial convencional, obteniéndose muestras con informadas por Anatomía Patológica compatible con Liposarcoma bien diferenciado.


Figura 2. (A) Tomografía
A B computarizada corte axial
mostrando ocupación tumo- ral completa del hemitórax inferior derecho, que con-
tacta anteriormente con el hemitórax izquierdo. (B) Resonancia magnética cor-
te coronal que evidencia la compresión y desplaza- miento del corazón y es-
tructuras vasculares del mediastino medio.
Diagnóstico:
Liposarcoma mediastínico primario gigante bien diferenciado (bajo grado)
Tratamiento y Evolución:
Tras valoración por el Servicio de Oncología, se descarta tratamiento quimio- radioterápico exclusivo y se contacta con Cirugía Torácica para valoración quirúrgica. El paciente presenta una fibrilación auricular de alta respuesta ventricular de inicio reciente y difícil manejo farmacológico, que junto con su mala situación funcional
respiratoria contraindican la cirugía en ese momento. Se realiza una arteriografía con
intención terapéutica para valorar embolización selectiva, que es desestimada tras comprobarse la ausencia de ramas arteriales adecuadas para dicho procedimiento. Tras el control de la arritmia cardiaca y una leve mejoría en la exploración funcional
respiratoria en los días siguientes, el paciente es intervenido a través de toracotomía lateral derecha, consiguiéndose la extirpación completa de una tumoración gigante de mediastino anterior e inferior de más de 35 cm de diámetro y de 4,5 Kg de peso que corresponde a un liposarcoma con base de implantación en seno cardiofrénico derecho y grasa prepericárdica. El material es remitido a Anatomía Patológica que confirma el diagnóstico previo de Liposarcoma de bajo grado.
El paciente ingresa en la Unidad de Cuidados Intensivos (UCI) para control postoperatorio. En las siguientes horas presenta edema pulmonar ex vacuo y fiebre alta, con inestabilidad hemodinámica que precisa noradrenalina en perfusión continua a dosis altas y antibioticoterapia empírica de amplio espectro. En los siguientes días no se objetiva repuesta al tratamiento empleado, presentando empeoramiento general, leucopenia intensa (pancitopenia) y mayor inestabilidad hemodinámica y respiratoria sin respuesta a noradrenalina, ni relleno con fracciones inspiradas de oxígeno (FI O2) altas, produciéndose un fracaso renal que precisa hemodiafiltración veno-venosa continua (HDFVVC) que no es bien tolerada por el paciente, produciéndose su fallecimiento.
-6-
“EPOC MODERADO CON FRECUENTES AGUDIZACIONES COMO FORMA DE PRESENTACIÓN DE UN CONDROSARCOMA TRAQUEAL”
AUTORES: Minguito De La Iglesia J, Peña Miguel MT, Pueyo Bastida AM, Gallardo
Romero JM.
Servicio de Neumología-Complejo Asistencial Burgos
Paciente varón de 75 años, exfumador hace 40 años, enolismo moderado, SCASEST con coronarias normales, HT Pulmonar (estimada PAPS 45), enfermedad de Crohn. Sin alergias medicamentosas conocidas. En tratamiento habitual con acenocumarol, clopidogrel, ramipril, atorvastatina, omeprazol y mesalazina.
Refiere en los últimos meses disnea de moderados esfuerzos y cuadros catarrales de repetición con tos productiva, hemoptisis ocasional y ruidos en el pecho. Tratado por su MAP con antibióticos y mucolíticos con evolución tórpida. Ingresa finalmente con insuficiencia respiratoria, fiebre, tos con expectoración purulenta y disnea de pequeños esfuerzos. Al ingreso:
Exploración Física: Orientado con lenguaje coherente. Cianosis pero normocoloreado con O2. Sat basal 74% que normaliza con O2. IMC 27. 39 º C. No flapping tremor. AC: normal. AP: leve hipoventilación con roncus en bases. No edemas.
Analítica: No poliglobulia (Hb 16 g/dl, 50% hto). Leucocitosis con desviación izquierda (12mil L con 88% N). Aumento de RFA (PCR 81, PCT 0.7). Láctico normal. Insuficiencia respiratoria (GA al ingreso (FiO2 24%): pH 7.4, pCO2 38, pO2 56, Bic
23, Sat 90%).
RX Tórax: sólo presenta condensación en LID sin derrames, discreta hiperinsuflación. Tras ser dado de alta con diagnóstico de neumonía neumocócica y probable EPOC vs hiperreactividad bronquial se instaura tratamiento con salmeterol/fluticasona e ipratropio.
Seguido en consultas externas se realiza Curva F-V que muestra discreta amputación del FEV1, interpretada como mala técnica al mostrar también duración insuficiente de la maniobra espiratoria. FEV1 1860 cc (61%), FVC 1860 cc (43%), FEV1/FVC: 97. (Revisado a posteriori no cumplía los 4 criterios de Rotmann para obstrucción fija intratorácica).
Reingresa a las 3 semanas en Medicina Interna por persistencia de la tos sin claro aumento de su disnea, pero refiriendo episodios de DPN. A la exploración sigue sin edemas. Con tratamiento habitual de EPOC agudizado y furosemida mejora y es dado de alta.
Reingresa aproximadamente 6 meses después nuevamente con insuficiencia respiratoria secundaria a una nueva neumonía y agudización secundaria de EPOC. Tras leve mejoría inicial con tratamiento antibiótico, broncodilatador en aerosol, corticoides sistémicos y oxigenoterapia se objetiva durante el ingreso estridor inspiratorio progresivo audible sin fonendo. Se realiza videofibrobroncoscopia de urgencia objetivándose una tumoración blanquecina dura endoluminal subglótica a 2 cms de cuerdas vocales que ocluye prácticamente el 90% de la luz traqueal, que se biopsia: “proliferación tumoral de diferenciación condroide, con núcleos con ligera variabilidad morfológica, leve hipercromasía focal, binucleaciones ocasionales y sin actividad mitótica. Dx: Condrosarcoma condral bien diferenciado, de bajo grado o de Grado I ”
Puestos en contacto con el Servicio de ORL se realiza traqueotomía reglada de urgencia. Se solicita escáner cérvico-torácico para estudio de extensión y PET para intentar confirmar naturaleza neoplásica de la lesión y completar despistaje de enfermedad metastásica, informados respectivamente como “tumoración sólida de 3.8 cms en eje anteroposterior que llega a infiltrar cartílago cricoides, con desplazamiento luz aérea esofágica. No adenopatías patológicas” y “captación única patológica SUV 4.7”. Se completa el estudio con esofagogastroscopia que descarta infiltración esofágica. Finalmente el servicio de ORL realiza resección endoluminal con láser estimada de 2/3 de la lesión, no habiendo vuelto a presentar ingresos ni clínica respiratoria
DISCUSIÓN:
Se estima que los tumores primarios malignos traqueales representan el 0,2% de los tumores del tracto respiratorio. El condrosarcoma traqueal ha sido diagnosticado mayoritariamente en varones adultos (edad media 65 años). Los síntomas predominantes suelen son disnea, tos, estridor, hemoptisis, ronquera y neumonía. Al presentar disnea, tos y ruidos respiratorios pueden confundirse con otras patologías respiratorias obstructivas como asma o EPOC agudizado, lo que lleva a un retraso medio diagnóstico de 15 meses.
La radiografía no muestra generalmente alteraciones, pudiendo observarse hiperinsuflación o tráquea en reloj de arena. En el scanner pueden mostrar calcificaciones, auque esto no es patognomónico. No se recomienda RM rutinariamente para completar el estudio.
El patrón oro para el diagnóstico es la Fibrobroncoscopia, que permite además la obtención de biopsias, recomendándose la presencia de personal entrenado en IOT
difícil y traqueotomía de urgencia. El aspecto macroscópico suele ser el de una
protrusión endoluminal recubierta de mucosa normal y bien delimitada, firme, de consistencia dura, homogénea y de color blanco o canela. Al microscopio es similar al condrosarcoma óseo, y puede desdiferenciarse a tumores de alto grado más agresivos y metastatizantes.
El tratamiento es la resección, vía endoscópica con láser o por resección quirúrgica completa con reconstrucción traqueal. El láser suele ser con intención paliativa (el tumor suele recidivar) o para disminuir masa tumoral para proceder en un segundo tiempo a la resección quirúrgica, el único tratamiento curativo. El condrosarcoma, especialmente el de bajo grado, no responde a la quimioterapia. Clásicamente se consideraban tumores radioresistentes, aunque los de asiento óseo y laríngeo parecen Responder a la radioterapia, por lo que pudiera tener un papel en el control de la recurrencia local o en el tratamiento paliativo.
ICONOGRAFÍA:
Figura 2: Broncofibroscopia
Figura 1: Curva Flujo-Volumen
Bibliografía:
1.Rotman HH et al. Diagnosis of upper airway obstruction by pulmonary funtion testing. Chest 1975
2.Milisavljevic D et al. Stridor as initial clinical presentation of tracheal condroma Acta
Otorrinolaringol Esp. 2010
3. Maish M et al. Chondrosarcoma arising in the trachea: a case report and review of the literature. J Thorac Cardiovasc Surgery. 2003
4. Aznar et al. Condrosarcoma crico-traqueal. Acta Otorrinolaringol Esp. 2001